Sáng 7/8, đã diễn ra cuộc họp trực tuyến khẩn của Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1 vaccine COVID-19 “made in Vietnam” Nano Covax và thông qua đánh giá giữa kỳ giai đoạn 2 của vaccine này.
Tiếp tục cho phép triển khai thử nghiệm lâm sàng vacccine Nano Covax giai đoạn 3 với mức liều 25mcg
Tại điểm cầu Bộ Y tế, GS.TS Trương Việt Dũng - Chủ tịch Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia chủ trì cuộc họp.
Các thành viên của Hội đồng đạo đức đã nghe đại diện Học viện Quân Y – đơn vị đang thực hiện thử nghiệm lâm sàng đại diện cho các đơn vị thử nghiệm báo cáo kết qủa thử nghiệm lâm sàng (TNLS) giai đoạn 1 vaccine Nano Covax cũng như báo cáo đánh giá giữa kỳ giai đoạn 2.

GS.TS Trần Văn Thuấn, GS.TS Trương Việt Dũng cùng một số thầy cô trong Hội đồng đạo đức Quốc gia và nhóm thử nghiệm vaccine Nano Covax tại điểm cầu Bộ Y tế Ảnh: Nguyễn Nhiên
Hội đồng đã thống nhất nghiệm thu kết quả TNLS giai đoạn 1 vaccine Nano Covax với dữ liệu theo dõi đến tháng thứ 6 kể từ liều tiêm đầu tiên của giai đoạn 1 trên 60 người tình nguyện với 3 mức liều 25 mcg, 50 mcg, 75 mcg.
Trên cơ sở cập nhật kết quả đánh giá giữa kỳ giai đoạn 2 đến thời điểm hiện tại, Hội đồng quyết định tiếp tục cho phép triển khai TNLS giai đoạn 3 với mức liều 25mcg theo đề cương nghiên cứu đã được phê duyệt.
Về thiết kế thử nghiệm lâm sàng giai đoạn 3 và phân tích dữ liệu về tính sinh miễn dịch trong đánh giá dữ liệu nghiên cứu lâm sàng vaccine phòng chống COVID-19.
Các nội dung trao đổi nhằm có thể nhanh chóng xem xét, thẩm định dữ liệu nghiên cứu TNLS vaccine COVID-19 đảm bảo tính khoa học, chuẩn mực chung trên những điểm cơ bản có tính quyết định.
“Người dân nóng lòng chờ vaccine một thì chúng tôi cũng nóng lòng hơn vì thế cố gắng khẩn trương và làm việc nghiêm túc, cùng với tham khảo ý kiến chuyên gia, các thành viên của Hội đồng thường xuyên cập nhật tài liệu về vaccine mới nhất nhằm có thêm dữ liệu tham khảo vào quá trình đánh giá. Chúng ta thúc đẩy nghiên cứu nhanh nhưng phải đảm bảo an toàn, hiệu quả và khách quan” - GS.TS Trương Việt Dũng - nhấn mạnh.
Xem xét nghiên cứu về tiêm mũi 3 vaccine Nano Covax
Tại cuộc họp Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia, Thứ trưởng Bộ Y tế Trần Văn Thuấn - Tổ trưởng Tổ công tác đặc biệt về nghiên cứu thử nghiệm lâm sàng, phát triển vaccine phòng COVID-19 tới dự để nghe, nắm bắt thêm các thông tin về tình hình triển khai nghiên cứu thử nghiệm lâm sàng vaccine Nano Covax.
Phát biểu tại đây, Thứ trưởng nhấn mạnh dịch bệnh diễn biến phức tạp, chiến lược vaccine đóng vai trò chủ chốt trong công tác phòng chống dịch.
Về chủ trương, Bộ Y tế hết sức ủng hộ và mong muốn có vaccine trong nước càng sớm càng tốt để chúng ta có thể tự chủ về vaccine.
Tuy nhiên khoa học là khoa học, chúng ta rút gọn thủ tục hành chính để nhanh chóng có vaccine trong nước nhưng cũng phải đảm bảo tính khoa học và khách quan.

Thứ trưởng Bộ Y tế Trần Văn Thuấn nhấn mạnh: Về chủ trương, Bộ Y tế hết sức ủng hộ và mong muốn có vaccine trong nước càng sớm càng tốt để chúng ta có thể tự chủ về vaccine. Ảnh: Nguyễn Nhiên
Theo Thứ trưởng Trần Văn Thuấn đây là cuộc họp hội đồng đạo đức đánh giá kết quả thử nghiệm lâm sàng pha 1 và giữa kỳ pha 2 hết sức khẩn trương, nghiêm túc, thể hiện rõ sự ủng hộ, quyết tâm, quyết liệt của Bộ Y tế đối với việc nghiên cứu phát triển vaccine phòng chống COVID-19 trong nước
“Chúng ta khẩn trương nhưng cần phải khoa học, chặt chẽ để đảm bảo số liệu đưa ra đủ tin cậy” - Thứ trưởng nhấn mạnh.
Bộ Y tế đồng tình với ý kiến của Chủ tịch Hội đồng về việc cần thành lập ngay tổ hỗ trợ, phân tích, đánh giá, giám sát số liệu và quy trình của 2 đơn vị tham gia nghiên cứu thử nghiệm lâm sàng, và phải có báo cáo trước ngày 14/8/2021.
Thứ trưởng Trần Văn Thuấn cũng đề nghị các đơn vị nhận thử như Học viện Quân y, Viện Pasteur Thành phố Hồ Chí Minh và đơn vị độc lập là Viện Vệ sinh dịch tễ Trung ương kết hợp với nhà sản xuất là Công ty Cổ phần công nghệ sinh học dược Nanogen: sau khi Hội đồng đã cho phép nghiệm thu kết quả giai đoạn 1 và giữa kỳ giai đoạn 2 phải khẩn trương hoàn thiện, đồng thời chuẩn bị ngay và gửi cho Hội đồng và Cục Khoa học Công nghệ và Đào tạo báo cáo pha 3a, gửi càng sớm càng tốt, ngay đầu tuần tới.
Trên cơ sở đó, kết hợp với kết quả của Tổ công tác, Thứ trưởng đề nghị Hội đồng tiếp tục họp vào ngày 15/8/2021 để đánh giá kết quả giai đoạn 3a.
Dựa trên kết quả đánh giá, đề nghị các thầy cô trong Hội đồng khuyến nghị các biện pháp khẩn thiết, cần thiết, hợp lý.
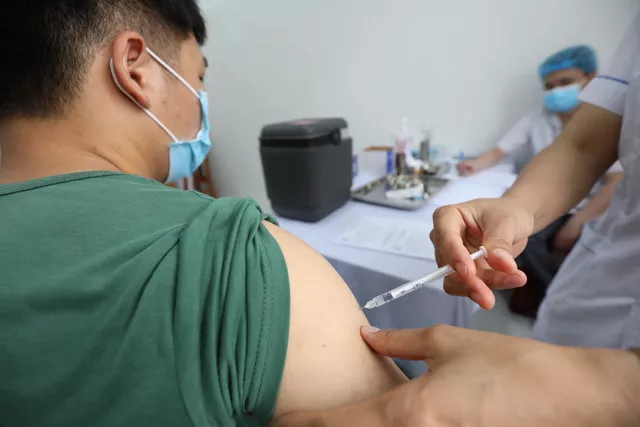
Tiêm thử nghiệm lâm sàng giai đoạn 3 vaccine Nano Covax cho người tình nguyện
Tại cuôc họp hôm nay, với đầy đủ các cơ quan nghiên cứu, Bộ Y tế đề nghị cân nhắc xem xét có tiến hành thêm 1 nghiên cứu bổ sung về việc tiêm mũi 3 vaccine Nano Covax hay không, bên cạnh đó xem xét bổ sung các chủng mới của virus Corona (như chủng Delta) vào nghiên cứu ở thời điểm thích hợp.
Cũng tại cuộc họp, Thứ trưởng Trần Văn Thuấn đề nghị Cục Khoa học Công nghệ và Đào tạo có công văn trả lời các tỉnh có công văn gửi Chính phủ, Bộ Y tế xin phép tiêm thử vaccine Nano Covax.
“Trong đó thể hiện rõ quan điểm của Bộ Y tế rất ủng hộ, tạo mọi điều kiện để các tỉnh tham gia thử nghiệm lâm sàng, tuy nhiên phải tuân thủ đúng theo các quy trình, quy định về thử nghiệm lâm sàng. Bộ Y tế rất không đồng ý việc lợi dụng ưu tiên thử nghiệm lâm sàng vào mục đích thương mại” - Thứ trưởng Trần Văn Thuấn nhấn mạnh.








![[Motion Graphics] Dấu hiệu nhận biết và cách phòng bệnh Chikungunya](https://cdn.baohatinh.vn/images/85e959bac00c7cf7806f7eb2ca448a295165930ea977049d87434f211d0fd5688dcb9850d9942e0ae7912b11c2659dfbc64db0ec857a408f890642ce478df764/bqbht_br_90.jpg)