Trong năm 2022, hơn 300 trẻ em, chủ yếu dưới 5 tuổi, ở Gambia, Indonesia và Uzbekistan, đã chết vì tổn thương thận cấp tính. Các ca tử vong có liên quan đến loại siro ho bị nhiễm độc, WHO cho biết trong tuyên bố ngày 23/1. Đây đều là các loại thuốc không kê đơn, có hàm lượng diethylene glycol và ethylene glycol cao.
“Đây là những hóa chất độc hại thường được sử dụng làm dung môi công nghiệp, chất chống đông, có thể gây tử vong sau khi uống một lượng nhỏ, không thường dùng trong thuốc”, WHO cho biết vaf cảnh báo Philippines, Timor Leste, Senegal và Campuchia có thể bị ảnh hưởng vì đang bày bán các loại thuốc này.
Tổ chức này kêu gọi 194 quốc gia phối hợp hành động để ngăn chặn các ca tử vong, bởi nhận định đây không phải sự cố riêng lẻ của bất cứ nước nào. Vì vậy, tổ chức kêu gọi các bên liên quan tham gia vào chuỗi cung ứng y tế và có hành động phối hợp ngay lập tức.
WHO đã phát cảnh báo vào tháng 10 năm ngoái và đầu tháng 1 năm nay, yêu cầu loại bỏ các loại siro ho Maiden Pharmaceuticals và Marion Biotech do Ấn Độ sản xuất khỏi kệ hàng. Đây là hai sản phẩm có liên quan đến các trường hợp tử vong ở Gambia và Uzbekistan.
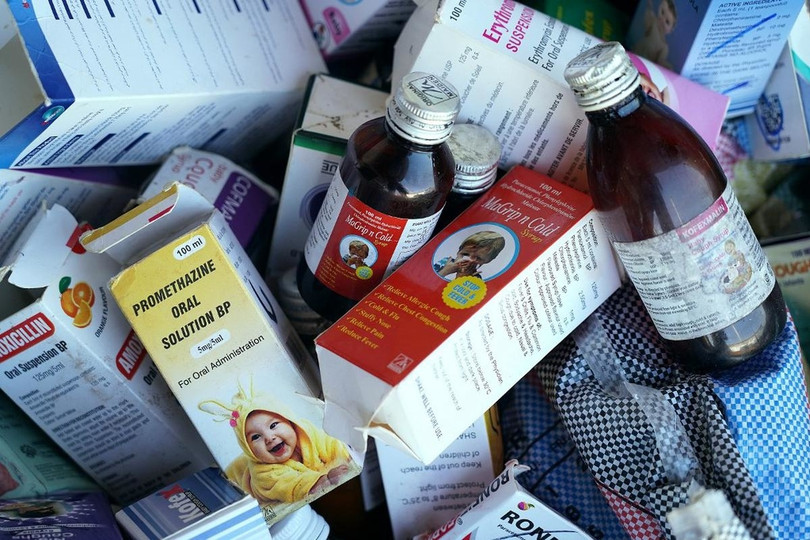
Một số loại siro ho được bày bán ở thành phố Banjul, Gambi, ngày 6/10. Ảnh: AFP
Năm ngoái, cơ quan cũng cảnh báo đối với siro từ 4 nhà sản xuất Indonesia là PT Yarindo Farmatama, PT Universal Pharmaceutical, PT Konimex và PT AFI Pharma. Các công ty liên quan phủ nhận sản phẩm nhiễm độc, một số từ chối bình luận trong khi các cuộc điều tra đang diễn ra.
WHO nhắc lại đề nghị loại bỏ sản phẩm khỏi hệ thống, kêu gọi các quốc gia kiểm soát các loại thuốc được bày bán, đảm bảo tất cả sản phẩm đều đã được phê duyệt. Tổ chức cũng yêu cầu chính phủ và các cơ quan phân bổ nguồn lực, kiểm tra các nhà sản xuất, tăng cường giám sát thị trường và hành động khi cần thiết; đồng thời khuyến nghị các nhà sản xuất chỉ mua nguyên liệu thô từ nhà cung cấp đủ tiêu chuẩn, kiểm tra sản phẩm kỹ lưỡng và lưu trữ hồ sơ quy trình. Các nhà cung cấp và phân phối nên kiểm tra dấu hiệu làm giả sản phẩm, chỉ phân phối hoặc bán ra các loại thuốc đã cấp phép.