Ngày 1/2, Bộ Y tế đã ban hành Quyết định số 983/QĐ-BYT phê duyệt có điều kiện vắc xin cho nhu cầu cấp bách trong phòng chống dịch bệnh COVID-19 theo quy định tại Điều 67, Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 của Chính phủ quy định chi tiết một số điều kiện và biện pháp thi hành Luật Dược, cụ thể: Vắc xin COVID-19 có tên là: Vắc xin AstraZeneca
Thành phần hoạt chất, nổng độ/hàm lượng: Mỗi liều (0,5ml) chứa: vắc xin COVID-19 (ChAdOxl-S tái tổ hợp) 5 x 10" hạt vi rút (vp).
Dạng bảo chế: Dung dịch tiêm.
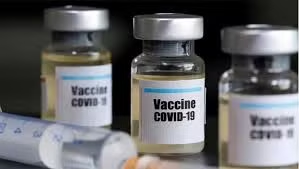
Vắc xin AstraZeneca là vắc xin COVID-19 đầu tiên được Bộ Y tế cấp phép lưu hành tại Việt Nam.
Quy cách đóng gói: Hộp 10 lọ, mỗi lọ chứa 8 liều, mỗi liều 0,5ml; Hộp 10 lọ, mỗi lọ chửa 10 liều, mỗi liều 0,5ml.
Tên cơ sở sản xuất - Nước sản xuất: Catalent Anagni S.R.L-Y; CP Pharmaceuticals Limited - Anh.l; IDT Biologika GmbH - Đức.
Cơ sở sản xuất có thể được thay đổi căn cứ vào khả năng cung cấp vắc xin tại thời điểm cơ sở nhập khẩu nộp Hồ sơ đề nghị cấp phép nhập khẩu vắc xin theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP.
Tên cơ sở đề nghị phê duyệt vắc xin: Công ty TNHH AstraZeneca Việt Nam
Quyết định của Bộ Y tế cũng cho biết, các điều kiện đi kèm việc phê duyệt vắc xin COVID-19 Vaccine AstraZeneca cho nhu cầu cấp bách trong phỏng, chống dịch bệnh Covid-19 được ban hành tại Phụ lục kèm theo Quyết định này.
Trách nhiệm của các đơn vị:
Cục Quản lý Dược có trách nhiệm: Cấp phép nhập khẩu vắc xin COVID-19 Vaccine AstraZeneca theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu.
Thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vắc xin nhập khẩu.
Cục Khoa học Công nghệ và Đào tạo có trách nhiệm làm đầu mối triển khai đánh giá lâm sàng tại Việt Nam về tinh an toản và tinh sinh miễn dịch của vắc xin COVID-19 Vaccine AstraZeneca,
Cục Y tế Dự phòng có trách nhiệm xây dựng kế hoạch tiêm chủng và tổ chức triển khai, hưởng dẫn tiêm chủng, giám sát trong quả trình tiêm chủng, theo dõi phản ứng sau tiêm chủng và tổ chức việc bảo cáo, tổng hợp thông tin, dữ liệu tiêm chủng vắc xin COVID-19 Vaccine AstraZeneca.
Viện Kiểm định Quốc gia vắc xin và sinh phẩm y tế có trách nhiệm tiến hành kiểm định vắc xin COVID-19 Vaccine AstraZeneca trước khi đưa ra sử dụng.
Quyết định này có hiệu lực kể từ ngày ký ban hành.
| Tại cuộc họp Thường trực Chính phủ chiều ngày 29/01/2021 tổ chức bên lề Đại hội Đảng lần thứ XII ở Trung tâm Hội nghị Quốc gia Mỹ Đình, GS.TS Nguyễn Thanh Long- Bộ trưởng Bộ Y tế thông tin: Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc của Bộ Y tế đã phê duyệt vắc xin phòng COVID-19 của Astra Zeneca cho trường hợp khẩn cấp phòng, chống dịch. Đây là vắc xin COVID-19 đầu tiên được Bộ Y tế cấp phép lưu hành tại Việt Nam. Cũng theo thông tin từ Bộ trưởng Bộ Y tế, Astra Zeneca đã cam kết cung cấp cho Việt Nam khoảng 30 triệu liều trong năm 2021, đồng thời Bộ Y tế vẫn tiếp tục làm việc với các đối tác để có thể tăng thêm số lượng vaccine cho Việt Nam. Dự kiến trong quý I năm nay, vắc xin của Astra Zeneca sẽ có mặt Việt Nam và được tiêm cho người dân. Ngoài ra, Bộ Y tế cũng chủ động, tích cực đàm phán với Pfizer, Moderna và một số nhà sản xuất vaccine khác để có thêm vắc xin cho Việt Nam. Đối với vaccine trong nước, Bộ Y tế tiếp tục chỉ đạo mạnh mẽ, sát sao và yêu cầu các đơn vị chủ động, khẩn trương triển khai việc nghiên cứu, thử nghiệm lâm sàng và tiến hành sản xuất để sớm có vắc xin phục vụ người dân. - Vắc xin Nanocovax do công ty Nanogen sản xuất đã hoàn thành thử nghiệm lâm sàng giai đoạn 1 và sẽ tiếp tục triển khai giai đoạn 2 ngay trong đầu tháng 02/2021.- Vắc xin Covivax của Viện Vaccine và Sinh phẩm y tế Nha Trang (IVAC) đã được khởi động thử nghiệm giai đoạn 1 ngày 21/01/2021 và dự kiến kết thúc vào cuối tháng 02/2021 để tiếp tục triển khai giai đoạn 2 trong tháng 3/2021 |











![[Infographic] Những điều cần biết về virus Hanta](https://cdn.baohatinh.vn/images/789daf41b959ecfd0c8affd56858f60c92355a0a6bc9e63a27244534dd13d26670ff5ce9256894d9b4b2d63a05d4b9d4/virus.jpg.avif)