Theo đó, tại quyết định số 62/QĐ-QLD, Cục trưởng Cục Quản lý Dược đã gia hạn gần 8.880 thuốc, nguyên liệu làm thuốc, vaccine và sinh phẩm y tế. Điều này có nghĩa là toàn bộ giấy đăng ký lưu hành của gần 8.880 thuốc, nguyên liệu làm thuốc, vaccine và sinh phẩm y tế được tiếp tục sử dụng từ ngày hết hiệu lực đến hết ngày 31/12/2024.
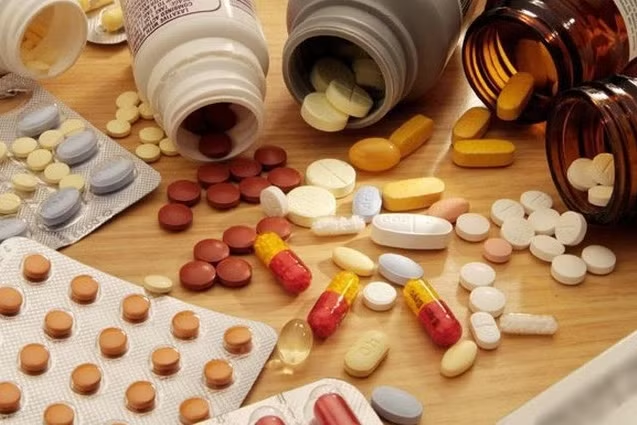
Trong đợt gia hạn đầu tiên của năm 2023 theo Nghị quyết số 80 của Quốc hội đã có gần 8.880 thuốc, nguyên liệu làm thuốc, vaccine và sinh phẩm y tế được Cục Quản lý Dược, Bộ Y tế gia hạn.
Trong số gần 8.880 thuốc, nguyên liệu làm thuốc, vaccine và sinh phẩm y tế được gia hạn lần này có 6.819 thuốc trong nước, 1.856 thuốc nước ngoài và 203 vaccine, sinh phẩm y tế.
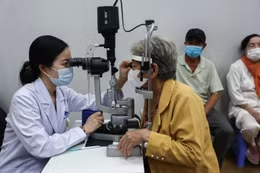
Các thuốc, nguyên liệu làm thuốc được công bố gia hạn đợt này có cả thuốc điều trị bệnh lý thông thường đến điều trị bệnh lý chuyên khoa đặc trị như tim mạch, tiêu hoá, tiểu đường, cơ xương khớp, hô hấp, nhiễm khuẩn, ung thư...
Trường hợp thuốc, nguyên liệu làm thuốc đã thực hiện thay đổi, bổ sung trong quá trình lưu hành hoặc có đính chính, sửa đổi thông tin liên quan đến giấy đăng ký lưu hành đã được cấp, doanh nghiệp xuất trình văn bản phê duyệt hoặc xác nhận của Cục Quản lý Dược với các cơ quan, đơn vị liên quan để thực hiện các thủ tục theo quy định pháp luật.
Trước đó, sáng 9/1/2023, dưới sự điều hành của Phó Chủ tịch Quốc hội Trần Thanh Mẫn, Quốc hội tiến hành biểu quyết thông qua Nghị quyết về việc tiếp tục thực hiện một số chính sách trong phòng, chống dịch và cho phép tiếp tục sử dụng giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hết thời hạn hiệu lực từ ngày 1/1/2023 mà chưa kịp gia hạn theo quy định của Luật Dược
Kết quả biểu quyết cho thấy, có 468/473 ĐBQH có mặt tham gia biểu quyết tán thành (chiếm 94,35%), Quốc hội chính thức thông qua Nghị quyết.
Liên quan đến vấn đề này, tại phiên thảo luận tổ của Kỳ họp bất thường lần thứ 2, Quốc hội khóa XV, sáng 6/1/2023, về đánh giá việc thực hiện quy định tại Nghị quyết số 30/2021/QH15 ngày 28/7/2021 Kỳ họp thứ nhất, Quốc hội khóa XV về các chính sách phòng, chống dịch bệnh COVID-19; đề xuất nội dung đưa vào Nghị quyết của Quốc hội về việc chuyển tiếp thực hiện một số chính sách theo quy định tại Nghị quyết số 30/2021/QH15 về các chính sách phòng, chống dịch bệnh COVID-19 và cho phép tiếp tục sử dụng giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hết thời hạn hiệu lực từ ngày 1/1/2023 mà chưa kịp gia hạn theo quy định của Luật Dược, Bộ trưởng Bộ Y tế Đào Hồng Lan thông tin, Bộ cũng đưa ra quy định rất rõ ràng là sau khi Quốc hội đồng ý, tất cả những tiêu chí, thuốc nào thuộc đối tượng gia hạn thì Bộ sẽ công khai trên Cổng thông tin điện tử để doanh nghiệp, người dân, cơ quan quản lý có thể theo dõi nhằm đảm bảo tính công khai, minh bạch.
Đặc biệt, người đứng đầu ngành y tế khẳng định, để giải quyết căn cơ vấn đề gia hạn giấy lưu hành thuốc, ngoài giải pháp trước mắt để đẩy nhanh tốc độ gia hạn thuốc thì Bộ đang xây dựng Luật Dược (sửa đổi). Trong đó cũng có đề xuất một số cơ chế mà quốc tế đang làm như việc gia hạn tự động thuốc. Dự thảo Luật Dược (sửa đổi) đã trình Chính phủ, hiện đang hoàn thiện hồ sơ để trình Bộ Tư pháp thẩm định và gửi sang đăng ký với Quốc hội trong thời gian tới.
Năm 2022, Cục Quản lý Dược, Bộ Y tế cũng đã gia hạn trên 10.000 thuốc, nguyên liệu làm thuốc, vaccine và sinh phẩm y tế.












![[Infographic] Những điều cần biết về virus Hanta](https://cdn.baohatinh.vn/images/789daf41b959ecfd0c8affd56858f60c92355a0a6bc9e63a27244534dd13d26670ff5ce9256894d9b4b2d63a05d4b9d4/virus.jpg.avif)